Các chất ức chế protease kháng retrovirus
Lịch sử: hội chứng suy giảm miễn dịch mắc phải (AIDS) được thừa nhận lần đầu tiên năm 1983 và do virus gây suy giảm miễn dịch người (HIV) gây ra. Mặc dù nhiều virus khác cũng là retrovirus, thuật ngữ "tác nhân kháng retrovirus" mô tả các tác nhân dùng điều trị nhiễm HIV. Nhóm chất đầu tiên được phép dùng điều trị HIV là các chất ức chế phiên mã ngược nucleosid (NRTI). Từ năm 1995, hai nhóm kháng retrovirus mới được giới thiệu: các chất ức chế protease (PI) và chất ức chế phiên mã ngược phi nucleosid (NNRTI), số tác nhân kháng retrovirus hiện đã gấp hơn 3 lần.
Với sự ra đời của các tác nhân mới này, việc điều trị HIV được cách mạng hóa và hiện bao gồm phối hợp "liệu pháp cocktail" hay liệu pháp kháng retrovirus hoạt tính cao (HAART). Các chuyên gia coi liệu pháp HAART là một trong số nhiều yếu tố làm tỷ lệ tử vong do AIDS ở Mỹ năm 1997 giảm 47%. Năm 1997, lần đầu tiên kể từ năm 1990, AIDS rời khỏi danh sách 10 nguyên nhân gây tử vong hàng đầu ở Mỹ, từ thứ 8 tụt xuống thứ 14. Đặc tính quan trọng nhất của HAART là khả năng phá vỡ HIV tại những giai đoạn khác nhau trong quá trình sao chép của virus. Các phác đồ kháng retrovirus hiện có không thể loại trừ được nhiễm HIV. Mục đích của liệu pháp điều trị HIV là đạt được mức giảm lượng virus tối đa và lâu bền, phục hồi và/hoặc bảo toàn chức năng miễn dịch, cải thiện chất lượng sống, và giảm bệnh suất cũng như tử suất liên quan đến HIV.
PI đầu tiên được cấp phép là saquinavir (Invirase(tm), viên nang gelatin cứng [HCG]) tháng 12 năm 1995. Các PI khác đã được cấp phép bao gồm ritonavir (Norvir(r)) (1996), Indinavir (Crixivan(r)) (1996), nelfinavir (Viracept(tm)) (1997) và amprenavir (Agenerase(tm)) (1999). Năm 1997, công thức mới của saquinavir (Fortovase(tm), viên nang gelatin mềm [SGC]) được cấp phép để tăng độ sinh khả dụng của saquinavir. Tháng 7 năm 1999, chế phẩm ritonavir mới được đưa ra thị trường; sản phẩm này được triển khai để khắc phục những khó khăn trong sản xuất trước đây. Nelfinavir là thuốc đầu tiên của nhóm này được phép dùng cho bệnh nhân khoa nhi; tiếp theo đó, ritonavir và amprenavir cũng được phép dùng cho trẻ em. Nhiều chế phẩm này đã được cấp phép thông qua chương trình "cấp phép nhanh" của FDA. Trong khi các PI có hoạt tính kháng virus cao, độ an toàn lâu dài của các chất này vẫn còn chưa xác định được và cùng với việc sử dụng rộng rãi các thuốc này người ta đang tìm ra những tác dụng phụ mới của chúng.
Các PI khác đang được nghiên cứu bao gồm trapanavir và ABT-378.
Cơ chế tác dụng: các PI ức chế protease HIV-1. Enzym này chịu trách nhiệm phân cắt chuỗi polypeptid gag và gag-pol của virus thành những chuỗi nhỏ hơn có chức năng, cho phép viron HIV hoàn thiện. Quá trình phân cắt và hoàn thiện diễn ra trong giai đoạn cuối cùng của vòng đời HIV. ức chế enzym protease giải phóng ra các mảnh virus rối loạn về cấu trúc và không gây nhiễm. PI có tác dụng trên cả tế bào nhiễm HIV cấp và mạn tính.
Tính kháng với các chất ức chế protease xuất hiện do đột biến trong các gen protease. Nhiều đột biến là do các PI khác nhau, bao gồm đột biến ở codon L90M do saquinavir, ở codon M461 và V82A/P do ritonavir và indinavir, và ở D30N do nelfinavir gây ra. Việc hình thành một số đột biến là cần thiết để có tính kháng cao với PI. Kháng chéo giữa các PI cũng đã được lưu ý; tuy nhiên, chưa thấy kháng chéo giữa các PI và các chất ức chế phiên mã ngược.
Đặc điểm phân biệt: có thể phân biệt các PI dựa vào đặc điểm dược lực học và tác dụng phụ. Thức ăn có thể ảnh hưởng đến sinh khả dụng của các PI. Người ta khuyên nên uống ritonavir, nelfinavir và saquinavir-HGC cùng với đồ ăn để tăng sinh khả dụng. Thức ăn làm giảm 77% mức indinavir; nên uống indinavir 1 giờ trước bữa ăn hoặc 2 giờ sau bữa ăn. Nên chia liều amprenavir, indinavir và ritonavir riêng rẽ với didanosin, ddI. Bữa ăn nhiều dầu mỡ có thể làm giảm 20% AU của amprenavir và nên tránh; nên uống amprenavir đều đặn cùng hoặc không cùng đồ ăn, tránh những bữa ăn giàu chất béo. Các công thức amprenavir cung cấp những liều vitamin E hằng ngày khá cao. Dung dịch amprenavir uống chứa 46UI vitamin E/ml và viên nang amprenavir chứa 109UI vitamin E/viên nang 150mg. Các công thức amprenavir không thể hoán đổi cho nhau theo mg/mg.
Tất cả các PI đều được chuyển hóa thông qua cytochrom P450 (CYP) 3A4 của gan và có tác dụng ức chế khác nhau đối với hệ thống này. Ritonavir là chất ức chế CYP3A4 mạnh nhất và ức chế CYP2D6 ở mức yếu hơn. Saquinavir là chất ức chế CYP3A4 yếu nhất và ở nồng độ thích hợp trên lâm sàng thuốc không ức chế chuyển hóa của các thuốc khác do CYP3A4 chuyển hóa. Amprenavir, indinavir và neldinavir ức chế CYP3A4 yếu hơn ritonavir. Nelfinavir và ritonavir cũng có tác dụng cảm ứng trên CYP3A4. Các PI tương tác với nhau, với các thuốc kháng retrovirus khác và với các thuốc khác. Các chất ức chế phiên mã ngược phi nucleosid (NNRTI) và các PI ảnh hưởng đến chuyển hóa của nhau; mức độ tuỳ thuộc vào sự phối hợp các thuốc. Do tác dụng của PI trên CYP3A4, người ta đã đánh giá nhiều phối thức đặc biệt của các PI để ngăn ngừa hoặc làm chậm sự xuất hiện kháng thuốc, để giảm liều, để có phác đồ liều thuận tiện hơn hoặc để giảm độc tính của PI. Ritonavir và saquinavir-HGC là những chất duy nhất được khuyến nghị dùng phối hợp. Mặt khác, không nên dùng công thức saquinavir-HCG mà nên kê đơn chế phẩm gelatin mềm.
Do các tác dụng của PI trên hệ CYP3A4, không nên dùng các thuốc sau cùng với PI: astemizol, cisaprid, các alkaloid cựa lúa mạch, lovastatin, midazolam, simvastatin, terfenadin hoặc triazolam. Ngoài ra, không nên dùng ritonavir cùng với amiodaron, bepridil, clozapin, flecainid, pimozid, propafenon hoặc quinidin. Không nên phối hợp rifampin hoặc cỏ thánh John với amprenavir, indinavir, nelfinavir hoặc saquinavir do cảm ứng chuyển hóa của PI và khả năng giảm tính kháng virus.
Tác dụng có hại: loạn dưỡng mỡ với sự phân bố lại mỡ, tăng mỡ máu và kháng insulin có liên quan với các PI ở những tần suất khác nhau. Những tác dụng có hại này có thể xảy ra đơn độc hoặc phối hợp. Đã có báo cáo về tăng đường huyết, bệnh đái đường mới khởi phát, nhiễm toan xêtôn do đái đường và bệnh đái đường nặng lên ở bệnh nhân dùng PI. Một số bệnh nhân bắt đầu dùng thuốc hạ đường huyết uống hoặc insulin và tiếp tục liệu pháp PI. Đường huyết cao có thể hồi phục nếu ngừng điều trị PI. Hiện chưa có số liệu để giúp quyết định tiếp tục hay ngừng liệu pháp PI; tuy nhiên phần lớn các chuyên gia khuyên nên tiếp tục liệu pháp PI nếu không bị đái đường nặng nguy hiểm đến tính mạng. Các triệu chứng của loạn dưỡng mỡ (còn được gọi là hội chứng giả Cushing) bao gồm béo vùng thân, chân tay gày, tích luỹ mỡ ở vùng gáy ("bướu trâu"), mặt gày và phì đại vú. Các phát hiện tương tự cũng đã được báo cáo ở bệnh nhân không dùng PI; tuy nhiên, số báo cáo ngày càng tăng từ khi các phác đồ có PI được sử dụng rộng rãi. Có ít số liệu về xử trí những triệu chứng này, nhưng người ta không khuyên giảm liều. Tất cả các PI đều có thể làm tăng mỡ máu, nhưng ritonavir làm tăng rõ rệt triglycerid và cholesterol, có hoặc không có biểu hiện loạn dưỡng mỡ trên lâm sàng. Hậu quả dài ngày của tăng mỡ máu hiện đang là mối lo ngại vì khả năng gây bệnh tim mạch và viêm tụy. Hiện chưa rõ hiệu quả của thay đổi chế độ ăn hoặc thuốc hạ lipid đối với bất thường lipid do PI gây ra.
Đã quan sát thấy tăng số đợt chảy máu tự phát ở bệnh nhân hemophilia điều trị bằng PI. Phần lớn các đợt xuất huyết là ở khớp hoặc mô mềm; tuy nhiên, đã có báo cáo về những đợt xuất huyết nặng bao gồm xuất huyết nội sọ và xuất huyết tiêu hóa.
Tất cả các PI đều gây không dung nạp ở đường tiêu hóa bao gồm buồn nôn, nôn và ỉa chảy. Đã thấy có thay đổi vị giác ở bệnh nhân dùng ritonavir, đặc biệt là dạng lỏng. Indinavir có thể gây sỏi thận, dẫn đến giảm chức năng thận hoặc suy thận và cần ngừng indinavir tạm thời. Bệnh nhân dùng indinavir cần uống ít nhất 1,5l nước/ngày để đảm bảo đủ nước và ngăn ngừa sỏi thận.
Tóm lại: việc điều trị bệnh nhân nhiễm HIV là rất phức tạp do tính khả dụng của nhiều tác nhân chống retrovirus và sự phát triển nhanh chóng của các chế phẩm mới. Mặc dù liệu pháp HAART là bước tiến bộ đáng kể trong điều trị HIV, nó vẫn chưa chữa khỏi được bệnh. Các yếu tố khác như giá thành cao, phác đồ phức tạp, sự tuân thủ của bệnh nhân và tương tác với các liệu pháp khác có thể hạn chế khả năng sử dụng các phác đồ HAART. Các hướng dẫn hiện nay về điều trị ban đầu nhiễm HIV khuyến nghị dùng 2 thuốc NRTI với một chất ức chế protease hoặc 2 NRTI với 1 NNRTI. Số liệu từ các nghiên cứu ngắn ngày cho thấy phối hợp 3 NRTI, một trong số đó là abacavir, có thể thay thế cho những lựa chọn điều trị ban đầu.
(Theo cimsi)
Mới hơn
- LƯƠNG Y NGUYỄN BÁ NHO KHẮC TINH CỦA BỆNH UNG THƯ
- Thầy thuốc đến từ Đề án 1816 hiến máu cứu người bệnh
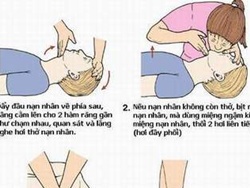
- Cách hô hấp nhân tạo và xoa bóp tim ngoài lồng ngực
- 65 năm chiến sĩ áo trắng
- Chiến thắng nỗi đau
- “Bắt bệnh” cho người chết
- “Giàng y tế” ở A Bung
- “Trái tim Đankô” của thầy thuốc làng HIV/AIDS
- Thần y trong nhà lao Côn Đảo
- Thành công từ ý chí và sự vươn lên không mệt mỏi
- Người bác sĩ giàu lòng nhân ái và sáng tạo
- Ở nơi “hạn hán nụ cười”
- Người Giàng
- “Hoa Đà” trên Cao nguyên đá
- Đông y và các bệnh thường gặp mùa lạnh
- Bệnh gút và điều trị gút trong đông y
- Bệnh nhồi máu cơ tim và bài thuốc chữa từ đông y
- Đông y điều trị rối loạn nhịp tim
- Chữa trĩ bằng Đông y
- Tự chữa bệnh trĩ bằng Đông y
- Đông y trị bệnh đau mắt đỏ
- Chữa trị rối loạn tiền đình theo Đông y
- Đông y trị chứng hoa mắt chóng mặt
- Khí công
- Mai hoa châm